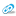Весьма распространенное мнение о том, что основным и оперативным источником глюкозы для любых жизненных проявлением служит гликоген печени, является ошибочным. На самом деле гликогенолиз включается, пожалуй, лишь при стрессе на фоне резкой активизации симпатоадреналовой системы, и действие его распространяется не больше, чем на 1,5-2,0 часа. В основном же, и в норме, и при патологии, и при напряженной адаптации глюкоза поступает в кровь с помощью глюконеогенеза (ГНГ).
Интенсификация же ГНГ возможна лишь при оптимальном поступлении необходимого для этого субстрата – аминокислот. В организме существует 7 белковых (аминокислотных) пулов или «источников»: 1) свободные аминокислоты крови, 2) аминокислоты эритроцитов, 3) аминокислоты белков свертывания и комплемента, 4) аминокислоты рыхлой соединительной ткани (коллагена и эластина), 5) аминокислоты печени, 6) аминокислоты мышц и 7) головного мозга. Идентификация состояния любого пула возможна лабораторными методами, но этим никто не занимается и «…никто не догадывается», к сожалению. А вопрос касается важнейшего механизма адаптации на все случаи жизни.
В обычных условиях человек между приемами пищи может обойтись кровяным пулом. Но если прием пищи откладывается и этот период затягивается, то подключается клеточный пул. Этим подключением и занимается гамма-глютамилтрансфераза (ГГТ). Она выполняет транспортную функцию. Транспортирует ГГТ именно те аминокислоты, которые, закончившись в одном пуле, заимствуются для ГНГ из другого пула, затем – из третьего, затем – из четвертого, и, наконец, из пятого.
Дело в том, что аминокислоты проникают в ткани против градиента концентрации, для чего нужен активный транспорт. Фермент обеспечивает энергозависимый транспорт АМК в клетки (35мг % в сыворотке и 520 мг% в тканях), поддержание уровня общего белка в крови в норме и патологии, а также разрешение диспротеинемии. Роль активного транспортировщика играет ГГТ. Это происходит при минимальном, но в то же время нормальном (табл.1) уровне ее активности, равном 20 МЕ/л. Любое повышение данного уровня свидетельствует об эпизодическом или постоянном заимствовании аминокислот из клеточных пулов. «Общепринятая норма» до 100 МЕ/л (что можно встретить в других руководствах) на самом деле указывает на физиологический или патологический дефицит аминокислот в целом организме. Уровни активности ГГТ вплоть до гигантских значений (до 1000 МЕ/л) говорят о мощном заимствовании аминокислот из тканей для дальнейшего ГНГ через АЛТ.
Так, например, при синдроме выжигания собственных белков на фоне длительной алкоголизации повышение ГГТ является маркером адаптации к алкогольному стрессору. У больного чрезвычайно активно заимствуются белки из собственных аминокислотных пулов. Чем выше активность ГГТ, тем лучше алкоголик переносит токсикоз, ведь его адаптивные способности выше. Образно выражаясь, высокая активность ГГТ – это широкие ворота в собственные белковые резервы.
Существует понятие онтогенетической ферментемии. Ее иллюстрацией может служить возрастная динамика ГГТ. При рождении уровень ГГТ может составлять онтогенетический максимум около 100 МЕ/л и выше. Это объяснимо необходимостью обеспечения интенсификации белкового метаболизма для роста и развития. К моменту полового созревания уровень активности ГГТ снижается до минимально оптимального уровня - 20 МЕ/л. Поэтому низкие значения активности ГГТ у 5-12-летних детей можно рассматривать как признак их онтогенетической незрелости. Кроме того, ГГТ может являться маркером малигнизации (перехода нормальной ткани в опухоль), а также аллергизации, что по смыслу не противоречит вышесказанному, так как опухоль является ловушкой аминокислот, способной довести организма до кахексии, а метаболизм гистамина и серотонина требует ГГТ.
Аллергизация – это ни что иное, как накопление производных гистидина в эозинофилах и серотонина в тучных клетках, что также, собственно, и представляет собой мощное перемещение аминокислот между клетками.
ГГТ относится к глютатионовой антиоксидантной системе. Ее роль резко возрастает при любом стрессе. ГГТ хорошо индуцируема, т.е. открыта для внешних воздействий, а также алкогольно-наркотически-медикаментозно зависима.
Таким образом, ГГТ является:
- аминокислотным насосом (транспортирует аминокислоты через
мембраны в клетки, обеспечивает адекватный уровень общего белка в
плазме);
- маркером малигнизации;
- маркером интоксикации (утилизирует потенциально токсичные
аминокислоты из плазмы);
- маркером аллергизации;
- маркером онтогенетической зрелости;
- антигенным компонентом;
- модулятором активности других ферментов;
- антиоксидантом (глутатион);
- активатором глюконеогенеза в условиях недостаточности инсулина;
- маркером регенерации и онкогенеза.
Наиболее выразительно ферментемия (свехнормальное повышение уровня активности фермента в крови) по ГГТ выявляется при алкоголизме, гепатитах, а также инфекционном мононуклеозе (ИМ).
В клинической практике Вы можете встретиться с такой ситуацией (табл. 1), когда активность АСТ в среднем повышена в пять, АЛТ – в девять, активность ЩФ в три, а ГГТ превышает нормальные показатели в 8,5 раз. Значительный разброс активности ферментов в «цитоплазматической» (АСТ, АЛТ) и в «мембранной» (ЩФ, ГГТ) парах заставляет по иному оценивать их роль. Активность поставляющего (ГГТ) фермента должна обеспечивать активность потребляющих (АСТ и АЛТ) ферментов и это зависит от состояния всех аминокислотных пулов, крайне индивидуально, этим и объясняется их значительный разброс.
Несмотря на высокую ферментемию, преимущественно «печеночных» ферментов, дополнительными методами обследования (УЗИ) патологии печени не было выявлено, что не удивительно, учитывая анамнез и возраст больных. В то же время «печеночный» коэффициент де Ритиса (АЛТ>АСТ) является показателем усиления перекачки аминокислот в глюкозу при лихорадочном синдроме. Гормональной основой стресса при инфекции является стероидогенез, который активирует ГНГ. ГНГ начинается с пирувата или щавелевоуксусной кислоты (ЩУК), образующихся из аланина и аспартата под действием соответственно АЛТ и АСТ. Именно глюкокортикоиды стимулируют 7-кратно образование АЛТ с периодом полужизни 84 часа и одновременной задержкой ее распада. Координировано с АЛТ увеличивается синтез аргиназы (конечный фермент цикла синтеза мочевины) с периодом полураспада 96 часов, что предполагает эффективную нейтрализацию образующегося аммиака после использования АМК. Признаком его активации является повышение уровня активности АЛТ, что установлено экспериментально и находит клиническое подтверждение.
Конечной целью регуляции метаболизма является поддержание энергетического гомеостаза, что реализуется через интенсификацию ГНГ в согласовании с ГАШ (глюкозо-аланиновым шунтом) (табл. 1). Не случайно в покое их активность абсолютно идентична и равна 20 МЕ/л. ГГТ ключевой фермент в системе детоксикации, и стабилизации пула АМК, дисбаланс которых является важнейшим механизмом токсикоза. Именно ГГТ является наиболее стабильным показателем и рост его активности наблюдается в ситуациях, когда отмечается рост активности трансаминаз.
Из классической биохимии известно, что существуют различные типы интенсивности обмена веществ – «быстрый» и «медленный» метаболизм. Это обуславливает разные метаболические сдвиги при лихорадочном синдроме, то есть «быстрый» метаболизм требует одних механизмов, а «медленный» - других, что также объясняет вариативность показателей. Одновременно существуют 4 уровня регуляции метаболизма: 1) субстратный, 2) модификационный (на уровне структуры ферментов), 3) белковый (через изоформы ферментов и геном) и 4) гормональный (синтез и распад). Молекулярная модификация связана с гликозилированием, а это влияет на взаимодействие фермента с мембранами при гормональной регуляции. Все это вместе и объясняет многообразие клиники, основанной на различных механизмах адаптации на уровне метаболизма. Очень низкий уровень ГГТ при беременности (надо охранять соматический пул для вынашивания плода), при менингококковой инфекции (много белков свертывания после мощного ДВС и их нужно утилизировать лихорадкой) и в онтогенезе (маркер детской инфантильности).