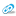ЛДГ – показатель окислительно-восстановительного потенциала крови, стабилизатор рН, маркер состояния эритроцитарного пула, компонент буферной системы, регулятор метаболических потоков, маркер анаэробного токсикоза и т. д. и т. п.
Сначала цифры: площадь капилляров печени равна 400 м2, в букве О может поместиться 100 эритроцитов, в эритроците 340000000 молекул гемоглобина, в клетке печени 1560 митохондрий (в 1 митохондрии 20 тыс. дыхательных ансамблей), 2.1013 молекул и 40 млрд. белков, в крови 750 г гемоглобина, скорость мозгового кровотока 750 мл/мин. А ведь 90 г глюкозы в сутки расходует мозг, 400г глюкозы синтезируется в печени и это количество за сутки дает 53 кг АТФ. Это погружение в микромир показывает, что требуется наличие фермента с макровозможностями, которыми и обладает ЛДГ. Через сердце в покое проходит 4л крови в 1 минуту, совершая полный оборот. Для функционирования организма необходимо «море крови» с характером горной реки, что и имеет организм в виде этой уникальной ткани. 1г массы человека за 1 час даёт в 10000 раз больше энергии, чем 1г Солнца и при этом 1л пота может снизить температуру на 10оС. А на коже 30 тыс. тепловых и 250 тыс. холодовых рецепторов для получения ранних сигналов о сохранении тепла. Всё это обеспечивает и стабильный, полифункциональный, до конца не понятный фермент ЛДГ, активность которого не опускается ниже 150 и не повышается выше 650 МЕ/л с манерой поведения физиологического типа, как рН или давление.
Общая активность лактатдегидрогеназы (ЛДГ) в покое составляет 250 МЕ/л и складывается из разных изоформ. ЛДГ обнаруживается во всех тканях животных и человека, особенно в сердечной и скелетных мышцах, эритроцитах, печени и почках. Молекула ЛДГ с мол. массой 140 000 представляет собой тетрамер, состоящий из одного или двух типов субъединиц Н и М, комбинации которых образуют 5 изоформ фермента: ЛДГ1, ЛДГ2, ЛДГ3, ЛДГ4, ЛДГ5 (рис.12). Изоферменты катализируют одну реакцию, но имеют различное строение (своеобразные биохимические синонимы). Остальные же изоформы менее органоспецифичны, но в определенной мере увязаны с почками, печенью и головным мозгом.
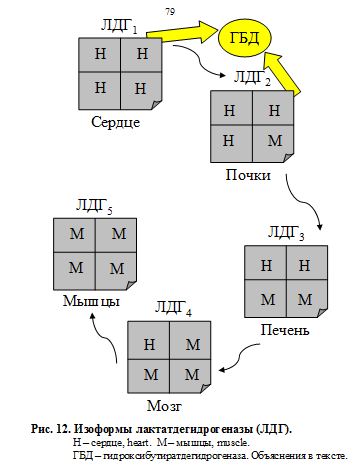
ЛДГ способна катализировать образование как тупикового токсичного лактата, так и вариативного пирувата и фактически выполнять буферную роль по отношению к пулу кетокислот - полифункциональных метаболитов. ЛДГ создает фонд кетокислот для последующего трансаминирования, т.е. фермент с большей активностью (активность ЛДГ равна 250 МЕ/л) создаёт широкие метаболические возможности для ферментов с меньшей активностью и более узкой специфичностью (АСТ – 30 и АЛТ – 20 МЕ/л). Жесткий интервальный уровень активности фермента в крови необходим для создания оптимальной интенсивности и направленности потока важнейших метаболитов в зависимости от складывающихся физиологических условий. Реакция превращения пировиноградной кислоты (ПВК) в молочную с участием ЛДГ5 (рис. 13) называется пируватгидрогенезированием, а сам фермент (ЛДГ5) в этом случае именуется «пируват-гидрогеназа». Обратный процесс катализируется тем же ферментом, но теперь его «официальное» название – лактатдегидрогеназа. С точки зрения ортодоксального химика данный термин неверен, но принят. Оба взаимообратных процесса равновесны и представляют собой единую саморегулирующуюся систему, поддерживающую конкретные процентные соотношения каждого компонента. Но меняется субстрат, и равновесие поддерживается «в другую сторону», «в пользу» продукта реакции (рис.). Фактически это система саморегуляции в крови важнейших потоков. В сердце же организму нельзя допустить образования молочной кислоты, иначе произойдет contractura – остановка сердца. Зато в скелетных мышцах это вполне допустимо. Ведь там МК, образуясь в анаэробных условиях при физической нагрузке, затем постепенно поступает в печень в цикл Кори, т.е. реверсивно превращается в глюкозу. От МК отщепляется два атома водорода, идет превращение МК в ПВК с участием ЛДГ1, схематично изображенное на рис. Часть пирувата, в свою очередь, идет по 1-му, 2-му и общему пути катаболизма глюкозы в цикле Кребса, а часть расходуется на образование глюкозы через глюконеогенез. Возможно также превращение ПВК в аланин (а затем – в белки) в ГАШ. На приведенном примере видно, насколько крепки организменные функциональные взаимосвязи между веществами, соединениями, их превращениями и физиологическими процессами. Все это объединяет организм в живую саморазвивающуюся систему, создает его целостность, формирует единство и содружественный ответ всех компонентов на постоянно меняющиеся условия окружающей среды. Это и есть – МЕТАБОЛИЗМ.
В физиологических условиях равновесие реакции, катализируемой ЛДГ, смещено в сторону образования лактата. В крови в норме содержание лактата 10-20 мг%, что на порядок выше, чем содержание пирувата 0.8-1.2 мг%. Восстановлением пирувата под действием ЛДГ завершается внутренний окислительно-восстановительный цикл гликолиза. Утомление мышц частично обусловлено развитием ацидоза в мышцах и при гликолизе из каждой нейтральной молекулы глюкозы образуются две молекулы молочной кислоты. В моче концентрация водородных ионов повышается в 800 раз. Использование искусственной гипергликемии у больных раком легкого с повышением глюкозы до 22-30 ммоль/л сопровождалось изменением соотношения анаэробных и аэробных фракций в пользу аэробных, что можно рассматривать как кратковременную адаптивную реакцию для более интенсивного сгорания избытка глюкозы. Периоды «полужизни» ЛДГ1 – 113±60 ч. и ЛДГ5 –10±2ч. Реакция катализируемая ЛДГ1 важнее для долгосрочного обеспечения энергетическими субстратами, а ЛДГ5 катализирует реакцию потенциально опасную с резким снижением уровня глюкозы, но более необходимую в экстренных ситуациях.
Онтогенетические сдвиги активности ЛДГ в тканях разнонаправлены: в печени с увеличением возраста происходит рост активности фермента, а в мозге и скелетных мышцах снижается. В почках и сердце активность не изменяется. У новорожденных активность составляет в среднем 175 МЕ/л и в течение первых 9 лет жизни снижается на 2.9 МЕ/л в год, затем падение активности на 8 МЕ/л в год в возрасте от 14 до 21 года. Контроль за активностью ЛДГ осуществляется не только на уровне транскрипции и трансляции, но и на уровне разрушения фермента. В миокарде ЛДГ1 разрушается в 22 раза быстрее чем в скелетной мышце, что может ограничивать сгорание глюкозы в сердце и экономить ее для других тканей.
ЛДГ играет ключевую роль в глюкозо-аланиновом цикле, где осуществляется интеграция углеводного и белкового обменов. ЛДГ оказывает регуляторное воздействие на цикл Кори, протекающий в мышцах и печени, катализируя конечную стадию гликолиза и начальную глюконеогенеза. Как и в мультиферментных комплексах на мембранах и эритроцитах в крови большое количество ферментов и малое субстратов при интенсивном использовании последних (лактат венозной крови 0,9-1,7 ммоль/л, пируват – 34-103 ммоль/л). Это наводит на мысль о возможности протекания реакций в крови для особой роли ферментов. Изменяя рН среды и, следовательно, направление всего одной ферментативной реакции можно получить разнообразные догормональные метаболические эффекты, которые приведут к изменению активности других ферментов и других видов обмена в среде их функционирования.
ЛДГ имеет постоянно высокий уровень активности в сыворотке, не опускаясь ниже 99 МЕ/л. Максимальная активность приходится на ЛДГ1,2, которая определяет высокую постоянную активность ЛДГ и зависит от полужизни фермента. Анаэробные фракции менее представлены в тканях, в большей степени деградируют и имеют более короткий период полужизни. Глюкоза является наиболее доступным для организма субстратом при разных условиях существования, а ключевой и регуляторный фермент метаболизма глюкозы должен иметь высокую активность и обладать определенным «резервом» для экстремальных ситуаций и поэтому его можно рассматривать как буферную систему.
ЛДГ имеет неабсолютную специфичность, иначе способен превращать и гидроксибутират из липидного обмена, т.е. влиять на соотношение углеводного и липидного обмена. Но это особая тема.