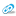Медики Первого МГМУ имени И.М. Сеченова выпустили обзор научных статей, в котором показали, каким образом атомы железа запускают процессы ферроптоза – программируемой смерти клетки. Статья ученых опубликована в журнале Free Radical Biology and Medicine.
Медики Первого МГМУ имени И.М. Сеченова выпустили обзор научных статей, в котором показали, каким образом атомы железа запускают процессы ферроптоза – программируемой смерти клетки. Статья ученых опубликована в журнале Free Radical Biology and Medicine.
Железо участвует во многих биологических процессах в качестве катализатора или окислителя. Также атомы железа содержатся во многих биологически активных структурах, например, в геме гемоглобина, где они выполняют функцию связывания кислорода. Впрочем, помимо жизненно важных процессов, атомы железа могут катализировать и вредные для клетки реакции и приводить к ее гибели.
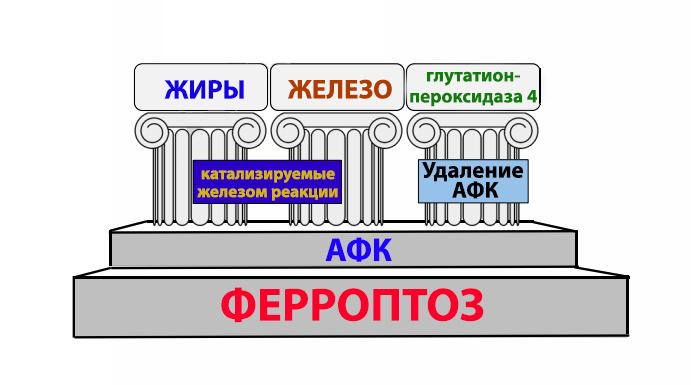
При накоплении железа в клетке оно начинает ускорять реакции перекисного окисления жиров (липидов), в ходе которых образуются активные формы кислорода (АФК), также называемые свободными радикалами. Эти частицы представляют собой атомы кислорода, имеющие один электрон на внешнем уровне. Этот факт обуславливает высокую окислительную способность АФК, благодаря чему они могут повреждать органеллы клеток и их стенки. Процесс гибели клеток, обусловленный накоплением в них атомов железа, называется ферроптозом.
Описанный выше механизм ферроптоза, связанный с действием АФК, не единственный. Ученые также выделяют второй путь, связывающий накопление железа в клетке с ее гибелью. Он заключается в уменьшении активности глутатионпероксидазы 4 – фермента, устраняющего перекисные соединения, которые являются источниками активных форм кислорода.
До сих пор оставалось неясным, какой из механизмов в какой степени влияет на ферроптоз. Чтобы продвинуться в решении этой проблемы, коллектив авторов, среди которых медик МГМУ имени И.М. Сеченова и его коллеги из США и Австрии, опубликовал обзор большого количества научных работ разных лет. Ученые выяснили, что наибольшую роль в ферроптозе играют процессы уменьшения активности фермента глутатионпероксидазы 4. Ранее считалось, что в ферроптозе, как и в других процессах программируемой гибели (апоптозе и некроптозе), ключевую роль играет процесс окисления жиров, катализируемый железом, в ходе которого образуются АФК. По словам авторов нового обзора, влияние реакции окисления жиров на гибель клеток было достоверно доказано только для апоптоза. Два других процесса программируемой гибели, согласно исследованиям, обусловлены другими протекающими внутри клетки ферментативными реакциями. В частности, ферроптоз, скорее, обусловлен уменьшением активности глутатионпероксидазы 4, задействованной в удалении активных форм кислорода из внутриклеточной среды.
«Большое количество экспериментальных данных показывает вклад строго контролируемых «зацикленных» железо-зависимых процессов роста клеток и повышения их выживаемости. Имеются также результаты, указывающие на роль железа в ферроптозе. Мы предложили вариант, при котором можно совместить эти два, казалось бы, противоположных процесса. Разрешение этой головоломки сильно зависит от идентификации белков, вызывающих ферроптоз, то есть ответственных за разрушение клеточной мембраны и следующую за этим гибель клетки», – говорит один из авторов работы, д.м.н., заведующий кафедрой патологии человека Сеченовского университета Сергей Болевич.