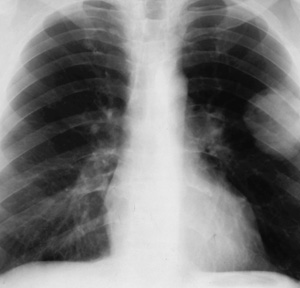
На прошедшем в Москве 15–17 ноября 2016 года Международном онкологическом конгрессе специалисты из РОНЦ им. Блохина рассказали о прорыве в диагностике и лечении рака легкого на основе молекулярно-генетического анализа опухоли.
Рак легкого занимает первое в мире место в структуре смертности от онкологических заболеваний как у мужчин, так и у женщин. В России из 60 тысяч ежегодно заболевающих раком легкого у 70–75 % опухоль выявляется в III–IV стадии, когда результаты лечения, как правило, заведомо неутешительны. У остальных же 25–30 % с ранними стадиями прогноз развития болезни до последнего времени оставался неясным, и около трети из них умирали в течение года после операции, несмотря на проведенное послеоперационное лечение.
Основной тип злокачественной болезни легких — так называемый немелкоклеточный рак легкого (HMPЛ), характеризующийся крайне агрессивным течением. По гистологическому строению он подразделяется на аденокарциному, плоскоклеточный, крупноклеточный, бронхиолоальвеолярный и др. Исторически в России большую часть случаев НМРЛ долгие годы составлял плоскоклеточный рак, однако в последние 35 лет аденокарцинома стала с ним вровень. Возможно, это связано с изменением состава сигарет. Корреляция между курением и раком для специалистов очевидна, как, скажем, для обывателя связь между громом и молнией. Но это не единственная возможная причина возникновения рака. К сожалению, нередко генетические мутации нередко возникают у людей, ведущих правильный образ жизни, — так называемый «невинный» рак.
Известно, что для злокачественных опухолей, в том числе и для НМРЛ, характерны многочисленные молекулярно-генетические нарушения, определяющие индивидуальность развития рака. Они влияют на клеточный цикл, темпы роста опухоли, локальную агрессивность и метастазирование, способность опухоли обеспечить себя собственным кровотоком, часто нарушают апоптоз — защитный процесс естественной программируемой гибели клетки.
К типичным для НМРЛ молекулярно-генетическим нарушениям относятся мутации генов, вызывающих патологическую стимуляцию непрерывного роста клетки, при этом часто выявляется повышенная экспрессия (усиленный синтез) некоторых белков. Иногда обнаруживаются признаки утраты активности генов, подавляющих опухолевый рост (так называемых супрессоров).
Однако на первых стадиях опухолевого процесса болезнь протекает бессимптомно. Большинство пациентов приходит к онкологам в уже запущенном состоянии, с жалобами на плохое самочувствие и разнообразную симптоматику. Чаще всего пациенты жалуются на кашель, осиплость, одышку, кровохарканье, боли в груди. При этом основным и наиболее эффективным методом, дающим реальный шанс на выздоровление при I-IIIA стадиях НМРЛ до сих пор считалась резекция легкого или его удаление с регионарными лимфатическими узлами. Такие тяжелые сопутствующие заболевания, как диабет или сердечно-сосудистые проблемы могут стать противопоказанием к операции. В этом случае применяются другие методы — лучевая терапия, радиочастотная абляция. Однако в результате лучевой терапии может проявиться токсичность, а радиочастотная абляция может осложниться кровотечением или пневмотораксом.
Но самая большая проблема — даже не все эти осложнения и противопоказания, а то, что у 30–50 % больных даже с ранними стадиями HMPЛ, несмотря на проведенное лечение, развивается рецидив, причем, как правило, он оказывается серьезнее первичного заболевания. Специалисты из РОНЦ им. Блохина около 16 лет назад озадачились вопросом: почему одни больные выздоравливают, а другие, имеющие тот же диагноз и аналогичное лечение, погибают?
Начиная с 2000-го года в онкоцентре началось молекулярно-генетическое изучение различных типов биоматериала, взятого во время операций, в результате чего удалось выявить ряд закономерностей, которые отличали одинаковые на первый взгляд опухоли. Оказалось, что они вовсе не одинаковы. Выяснилось, что любая опухоль, на какой бы стадии она ни находилась и к какому бы типу ни относилась, ведет себя индивидуально. Константин Лактионов, доктор медицинских наук, руководитель хирургического отделения клинических биотехнологий РОНЦ им. Блохина, заместитель директора РОНЦ по науке, для наглядности проводит аналогию: стоит машина, накрытая брезентом, и понять, что под ним — «Москвич» или «BMW» — возможно, только приоткрыв брезент. Так и опухоль: выяснить, что она собой представляет, можно, лишь проведя соответствующие исследования. Логично предположить, что и подходы к лечению не должны быть общими для всех.
Коллективу научных сотрудников РОНЦ им. Блохина под руководством директора Центра, торакального хирурга, академика РАН и РАМН Михаила Давыдова в течение этих лет удалось выработать алгоритмы диагностики и лечения опухоли. Аналогичные работы в мире единичны. Потребовался целый ряд исследований — например, многофакторный анализ клинико-морфологических и молекулярно-биологических особенностей первичной опухоли, в результате чего была выделена группа больных с биологически неблагоприятным прогнозом течения заболевания. Затем была оценена результативность адъювантной (послеоперационной) химиотерапии у больных с неблагоприятным прогнозом — живут ли они дольше с ней или без нее. Были важны и многие другие показатели — скажем, определение экспрессии молекулярно-биологических маркеров, ассоциированных с устойчивостью к тем или иным препаратам, определение корреляции фактической и прогнозируемой эффективности стандартной химиотерапии, а также целесообразности проведения тех или иных этапов лечения.
Была также выработана последовательность методов, позволяющих с максимальной достоверностью распределить больных раком легкого на группы благоприятного и неблагоприятного биологического прогноза течения заболевания. Пациентам с неблагоприятным биологическим прогнозом (продолжительность жизни не превышает трех лет) показана послеоперационная химиотерапия даже при I стадии — вопреки существующим стандартам. Очень важно, что удалось уйти из «серой» зоны — иначе говоря, больных с неопределенным, «непонятным» прогнозом просто нет.
150 пациентов РОНЦ в ходе радикальной операции по поводу рака легкого подверглись молекулярно-генетическому анализу опухоли, после чего получили высоко точный прогноз и рекомендации последующего лечения, а затем в течение пяти-шести лет за ними наблюдали специалисты. Сделанный прогноз полностью себя оправдал. Те пациенты, которые получили благоприятный прогноз, могут динамически наблюдаться у врачей, не проходя никаких дополнительных видов лечения. Как правило, они наблюдаются в онкоцентре в течение пяти лет, после чего снимаются с учета как выздоровевшие. А те, у которых прогноз оказался неблагоприятным, получают таргетные препараты, химиотерапию и (или) онкоиммунотерапию, которая сегодня также высоко эффективна и способна продлить жизни пациента на три-пять и более лет, в то время как раньше для пациентов с таким диагнозом прогноз по продолжительности жизни не превышал одного года.
«В последние десятилетия онкологи во всем мире столкнулись с проблемой химиорезистентности злокачественных опухолей при назначении стандартных режимов лечения, — объясняет академик Михаил Давыдов. — Возможный вариант решения проблемы — использование результатов наших исследований. Разработанная нами маркерная панель охватывает все современные схемы лекарственного лечения и позволяет персонализировать лечебную тактику при раке легкого».
Наталия Лескова
обозреватель информационно-образовательного портала MedBook.ru